Mathilde Dupré, Manon Marc et Jean-François BussièresComment citer cet article : Dupré M, Marc M, Bussières JF. Efficacité de 6 scénarios de décontamination de bras de fauteuils contaminés volontairement au cyclophosphamide. Can J Hosp Pharm. 2024;77(4):e3588. doi: 10.4212/cjhp.3588
RÉSUMÉ
Contexte
Les bras de fauteuils en clinique externe d’oncologie sont fréquemment contaminés au cyclophosphamide.
Objectif
Évaluer l’efficacité de scénarios de décontamination.
Méthodologie
Il s’agit d’une étude descriptive de type simulation de 6 scénarios de décontamination d’une surface de tissu en silicone contaminée avec 10 μg de cyclophosphamide. Les produits de décontamination testés (ammonium quaternaire, peroxyde d’hydrogène 0,5 %, détergent 0,005 % et hypochlorite de sodium 0,5 %) ont été utilisés avec des lingettes de microfibres. La contamination résiduelle a été mesurée à l’aide d’un système de chromatographie liquide ultraperformante et de spectrométrie de masse en tandem, avec des limites de détection et de quantification du cyclophosphamide identiques (0,0006 ng/cm2).
Résultats
Parmi les 59 échantillons, 3 blancs étaient négatifs, 5 ont permis la mesure du taux de récupération (93,7 ± 4,6 % [écart-type]) et 51 étaient expérimentaux. L’efficacité moyenne des agents était supérieure ou égale à 99,79 %. Quel que soit l’agent utilisé, l’efficacité était de 99,30 ± 1,20 % après un seul nettoyage (n = 18), 99,90 ± 0,15 % après 2 (n = 18) et 99,95 ± 0,06 % après 3 (n = 15).
Conclusions
Six scénarios de décontamination se sont avérés efficaces. La répétition du nettoyage a augmenté de façon marginale l’efficacité de la décontamination.
Mots-clés: cyclophosphamide, décontamination, simulation
ABSTRACT
Background
The arms of chairs in outpatient oncology clinics are frequently contaminated with cyclophosphamide.
Objective
To evaluate the effectiveness of decontamination scenarios.
Methods
This was a descriptive simulation-type study of 6 decontamination scenarios of a silicone fabric surface contaminated with 10 μg of cyclophosphamide. The decontamination products tested (quaternary ammonium, 0.5% hydrogen peroxide, 0.005% detergent, and sodium hypochlorite 0.5%) were applied with microfibre wipes. Residual contamination was measured using an ultra-performance liquid chromatography-tandem mass spectrometry system with identical cyclophosphamide detection and quantification limits (0.0006 ng/cm2).
Results
Among the 59 samples, 3 blanks were negative, 5 allowed measurement of the recovery rate (93.7% [standard deviation 4.6%]), and 51 were experimental. The average efficiency of the agents was greater than or equal to 99.79%. Regardless of the agent used, effectiveness was 99.30% (SD 1.20%) after 1 cleanse (n = 18), 99.90% (SD 0.15%) after 2 cleanses (n = 18), and 99.95% (SD 0.06%) after 3 cleanses (n = 15).
Conclusion
The 6 decontamination scenarios were effective. Repeated cleaning marginally increased the effectiveness of decontamination.
KEYWORDS: cyclophosphamide, decontamination, simulation
On reconnaît les risques associés aux médicaments dangereux depuis plus de deux décennies1. Un médicament dangereux comporte des risques de cancérogénicité, de tératogénicité, de mutagénicité, de toxicité pour des organes ou pour la reproduction.
Au Canada, plusieurs provinces ont encadré l’utilisation des médicaments dangereux en produisant des lignes directrices et des recommandations2–8. Ces documents indiquent l’importance de protéger les travailleurs de la santé et d’assurer un entretien régulier des zones potentiellement contaminées aux médicaments dangereux en utilisant différentes stratégies de décontamination.
De nombreuses études ont démontré la présence de traces de médicaments dangereux, et particulièrement de médicaments cytotoxiques, dans l’environnement9. Des traces de médicaments dangereux ont notamment été mesurés à différents endroits de la pharmacie et des zones de soins aux patients. Pinet et al. ont publié les résultats de leur programme canadien de surveillance environnementale de traces d’antinéoplasiques en 202210. Dans les 124 hôpitaux participants, les auteurs ont observé principalement la présence de traces de cyclophosphamide (405/1445, 28 %), de gemcitabine (347/1445, 24 %) et de platines (71/756, 9 %).
Parmi les endroits fréquemment contaminés, on note les bras de fauteuils de clinique externe utilisés pour l’administration d’antinéoplasiques. Pinet et al. ont rapporté la présence de traces d’au moins un médicament dangereux sur les bras de fauteuils à raison de 81 % (97/120) des prélèvements effectués, dont la présence de traces de cyclophosphamide sur ces bras à raison de 74 % (89/120) des prélèvements effectués10. La quantité de cyclophosphamide mesurée sur les bras de fauteuils était de 0,0202 ng/cm2 (75e percentile), de 0,0611 ng/cm2 (90e percentile) et de 0,8861 ng/cm2 (max).
Afin de réduire la contamination des bras de fauteuils utilisés en clinique externe, nous nous sommes intéressés à une simulation entourant la décontamination de bras de fauteuils.
Il s’agit d’une étude descriptive de type simulation. L’objectif était d’évaluer l’efficacité de 6 scénarios de décontamination de bras de fauteuils contaminés volontairement au cyclophosphamide.
L’étude a été menée au CHU Sainte-Justine, Montréal (Québec). Les manipulations ont été effectuées dans une enceinte de sécurité biologique (ESB) (classe II, NuAire). Cette ESB a été préalablement décontaminée avec un protocole en 8 étapes.
Un rouleau de tissu neuf (100 % silicone sur une base tricot/polyester, bleu, Designtex) a été découpé en pièces de 600 cm2. Chaque pièce de tissu a été délibérément contaminée avec 10 μg (0,5 mL après redilution) de cyclophosphamide (Procytox, Baxter Corporation). À partir d’une solution primaire de cyclophosphamide de 1000 mg/50 mL (concentration de 20 mg/mL), nous avons prélevé 2,5 mL (50 mg) qui ont été ajoutés à 47,5 mL de chlorure de sodium 0,9 % dans une fiole vide de 50 mL pour une concentration de 1 mg/mL. À partir de cette fiole, nous avons prélevé 1 mL (1 mg) qui a été ajouté à 49 mL de chlorure de sodium 0,9 % dans une fiole vide de 50 mL pour une concentration finale de 0,02 mg/mL. Par la suite, nous avons prélevé un volume de 0,5 mL (0,01 mg ou 10 μg) pour chaque seringue utilisée pour la simulation. Cette quantité a été déposée et répartie sur la surface en 5 points pour chaque simulation.
Six scénarios de décontamination ont été testés avec un seul nettoyage, puis 2 et ensuite 3 nettoyages. Quatre produits de décontamination sous forme liquide ont été utilisés (ammonium quaternaire (DR-100, InnuScience), peroxyde d’hydrogène 0,5 % (Oxivir, Diversey Global), détergent 0,005 % (Nu-Action 3, SaniDépôt), hypochlorite de sodium 0,5 % (Zochlor, Glen Martin Limited)) et un en lingettes commerciales (peroxyde d’hydrogène, (Oxivir, Diversey Global)). Un sixième scénario de décontamination avec un seul nettoyage et 2 nettoyages a été effectué en utilisant une combinaison de 2 produits liquides (détergent 0,005 % (Action 3) et hypochlorite de sodium 0,5 %). Les scénarios ont été effectués en triplicata.
Pour chaque décontamination, une lingette en microfibres (Micronsolo, Vileda) a été utilisée selon les procédures usuelles d’entretien de l’équipe d’hygiène et salubrité de l’établissement de santé. Chaque lingette de nettoyage a été imbibée avec le produit de lavage applicable selon le scénario dans un bac. Chaque lingette était recouverte de liquide, puis essorée à la main par le manipulateur pour éliminer l’excédent de liquide et ensuite pliée en 2. Trois passages successifs étaient effectués sur la surface à décontaminer en utilisant 3 côtés de la lingette. Après décontamination, un temps de séchage de 3 minutes était chronométré avant l’échantillonnage. La lingette commerciale a été utilisée telle quelle.
Un test de récupération en quintuplicata et 3 mesures à blanc ont été effectués. Le test de récupération permet de vérifier la capacité de récupérer la quantité de cyclophosphamide déposée sur la surface évaluée, sans nettoyage. La mesure est répétée 5 fois pour obtenir un taux de récupération moyen. Les mesures à blanc sont effectuées sur des surfaces non contaminées et non nettoyées. Trois mesures ont été effectuées afin de confirmer l’absence préalable de contamination.
Tous les prélèvements ont été analysés à l’aide d’un système de chromatographie liquide ultra-performante et de spectrométrie de masse en tandem. Les limites de détection (LOD) et de quantification (LOQ) du cyclophosphamide étaient identiques (0,0006 ng/cm2).
Le taux d’efficacité (moyenne, écart-type) a été calculé selon la méthode suivante: concentration de cyclophosphamide mesurée par l’approche analytique convertie en ng/cm2 divisée par la quantité totale mesurable de cyclophosphamide ajustée avec le taux de récupération (c.-à-d. 10 μg ou 10 000 ng/600 cm2 déposé par simulation = 16,67 ng/cm2 × 0,937 de récupération = 15,62 ng/cm2).
Cinquante-neuf échantillons ont été prélevés (3 blancs, 5 taux de récupération et 51 expérimentaux). Le taux de récupération était de 93,7 ± 4,6 %. Les 3 échantillons à blanc étaient négatifs.
Le taux moyen d’efficacité des produits de décontamination était supérieur ou égal à 99,79 % à l’exception de la lingette commerciale (98,80 %). Quel que soit l’agent utilisé, le taux d’efficacité était de 99,30 ± 1,20 % après un seul nettoyage (n = 18), de 99,90 ± 0,15 % après 2 nettoyages (n = 18) et de 99,95 ± 0,06 % après 3 nettoyages (n = 15).
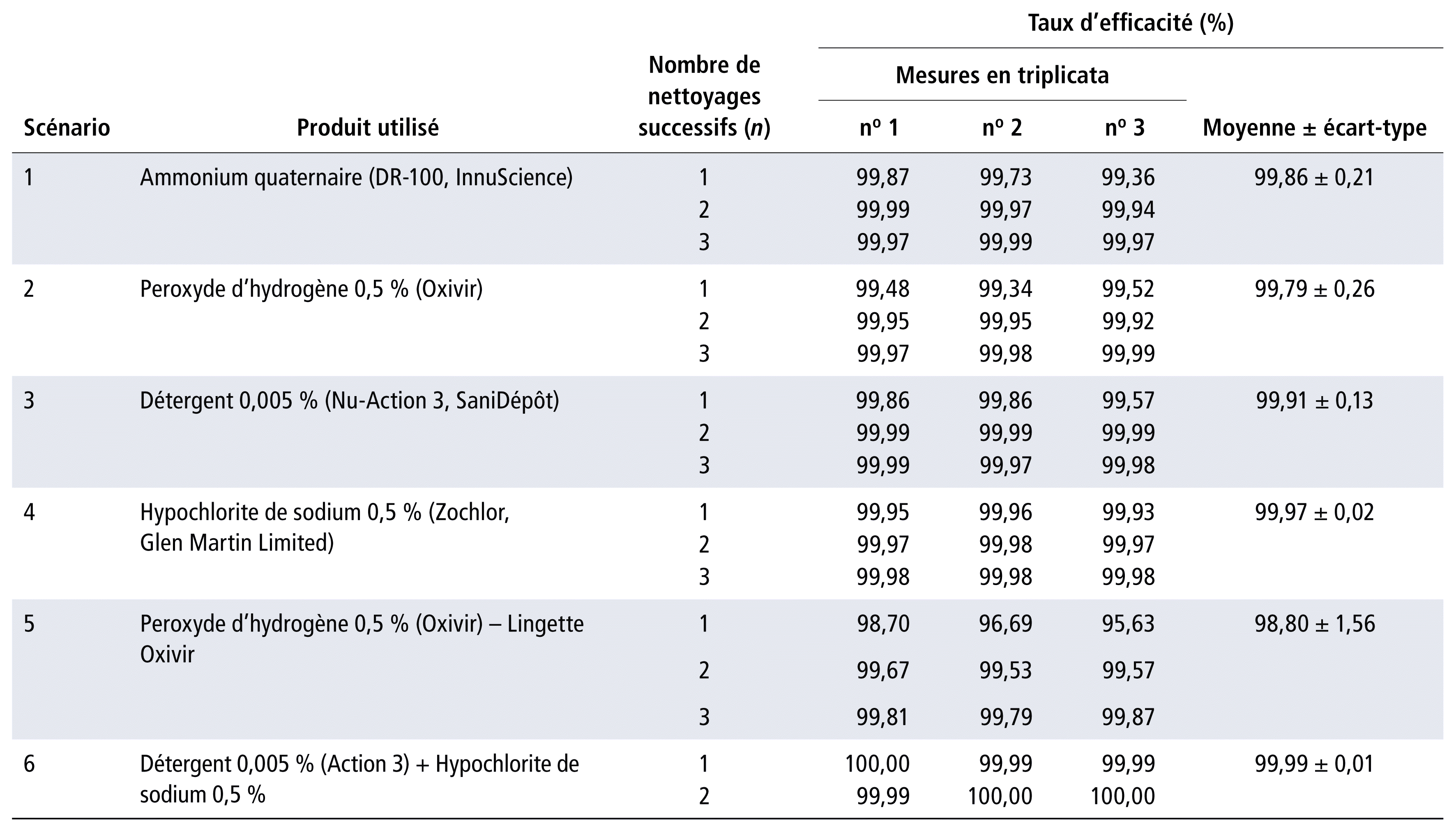
Le tableau 1 présente un profil de l’efficacité de 6 scénarios de décontamination.
TABLEAU 1 Profil de l’efficacité de 6 scénarios de décontamination de bras de fauteuils contaminés volontairement au cyclophosphamide

Cette étude évalue l’efficacité de 6 scénarios de décontamination de bras de fauteuils contaminés volontairement avec 10 μg de cyclophosphamide. Cette quantité de cyclophosphamide a été retenue parce qu’elle correspond à une valeur précédemment utilisée dans la littérature et qu’elle tient compte de la sensibilité de la méthode analytique
Les 5 produits de décontamination utilisés sont très efficaces pour éliminer presque toute la quantité de cyclophosphamide déposée volontairement sur une surface en tissu. Palamini et al. ont obtenu des taux similaires d’efficacité à la suite d’une contamination volontaire de cyclophosphamide sur une surface en acier inoxydable11. En revanche, Queruau Lamerie et al. ont obtenu des taux d’efficacité variables, de 80 % à 98 % selon le produit de décontamination utilisé et le médicament dangereux évalué12. Bien que le taux d’efficacité de la lingette de peroxyde d’hydrogène soit un peu moins élevé que les autres produits, le nombre limité de mesures ne permet pas de conclure à une différence significative entre les produits évalués.
Dans l’étude de 2022 du programme de surveillance environnementale de médicaments dangereux en établissement de santé, le 75e percentile de cyclophosphamide mesuré sur les bras de fauteuils correspondait à une valeur de 0,0202 ng/cm2. Afin de mettre en perspective les résultats de notre simulation, les quantités résiduelles de cyclophosphamide mesurées variaient de 0,001 à 0,678 ng/cm2. Ainsi, les valeurs résiduelles mesurées dans notre simulation sont beaucoup plus élevées que les traces mesurées dans le programme canadien de surveillance. Au quotidien, le personnel soignant qui constate une contamination (p. ex., une fuite de tubulure, une goutte qui s’écoule d’une seringue au branchement à la tubulure), procède généralement au nettoyage sans délai.
Soubieux et al. ont rapporté une efficacité accrue correspondant au nombre de nettoyages à la suite de la contamination volontaire au cyclophosphamide d’une surface d’enceinte biologique en acier inoxydable13. Notre étude semble indiquer une telle tendance, bien que l’efficacité additionnelle en fonction du nombre de nettoyages soit limitée. Il n’existe pas de données sur la fréquence optimale de nettoyage des bras de fauteuils. Compte tenu des risques de contamination issus notamment de l’administration de produits par voie intraveineuse, il apparaît raisonnable de nettoyer le bras de fauteuil après chaque patient, même si un piqué a été utilisé pour protéger la surface du bras de fauteuil du patient.
Plusieurs facteurs peuvent influencer l’efficacité de stratégies de décontamination, notamment le choix du produit ou des combinaisons de produits, le temps de contact, le type de lingette utilisé pour nettoyer la surface, la nature de la surface à décontaminer ainsi que son usure et le respect de la technique de décontamination. Simon et al. ont observé un taux d’efficacité variable, de 84,3 % à 100 %, selon le produit utilisé et la technique de nettoyage utilisée14.
Cette étude comporte des limites. L’étude est menée sur un seul type de tissu neuf. La surface utilisée est conforme aux consignes de la méthode analytique (600 cm2) et permet de vérifier l’efficacité des agents utilisés. Toutefois, en pratique, un bras de fauteuil présente une surface étroite et longue et la contamination peut survenir n’importe où sur le bras. D’autres tissus, neufs et usagés, pourraient être évalués. De même, une simulation de vrais bras de fauteuils pourrait aider à mieux comprendre la persistance de la contamination observée sur cette surface dans le programme canadien de surveillance.
Cinq produits de décontamination sont très efficaces pour retirer le cyclophosphamide déposé volontairement sur un tissu de bras de fauteuils. La répétition du nombre de nettoyage augmente de façon marginale l’efficacité de décontamination.
1 NIOSH Alert. Preventing occupational exposures to antineoplastic and other hazardous drugs in health care settings. Department of Health and Human Services, Centers for Disease Control and Prevention, National Institute for Occupational Safety and Health; septembre 2004 [consulté le 4 janvier 2024]. Disponible à: https://www.cdc.gov/niosh/docs/2004-165/pdfs/2004-165.pdf
2 Model standards for pharmacy compounding of hazardous sterile preparations. Association nationale des organismes de réglementation de la pharmacie; 2016 [consulté le 4 janvier 2024]. Disponible à: https://www.napra.ca/wp-content/uploads/2022/09/NAPRA-Mdl-Stnds-Pharmacy-Compounding-Hazardous-Sterile-Preparations-Nov-2016-Revised-b.pdf
3 Safe work practices for handling hazardous drugs. Worksafe BC; décembre 2023 [consulté le 4 janvier 2024]. Disponible à: https://www.worksafebc.com/en/resources/health-safety/books-guides/best-practices-safe-handling-hazardous-drugs?lang=en
4 Handbook of occupational hazards and controls for pharmacy workers. Gouvernement de l’Alberta; 2011 [consulté le 4 janvier 2024]. Disponible à: https://open.alberta.ca/dataset/handbook-of-occupational-hazards-and-controls-for-pharmacy-workers/resource/2bb42e14-f918-4235-8aec-d8f8da6a2ac0
5 Chemicals, dangerous goods and hazardous substances. Gouvernement de Saskatchewan, Occupational Health and Safety; 2021 [consulté le 4 janvier 2024. Disponible à: https://www.saskatchewan.ca/business/safety-in-the-workplace/hazards-and-prevention/chemicals-dangerous-goods-and-hazardous-substances#cytotoxic-drugs
6 Pharmacist administration of hazardous medications. College of Pharmacists of Manitoba; s.d. [consulté le 4 janvier 2024]. Disponible à: https://cphm.ca/wp-content/uploads/Resource-Library/Expanded-Scope/Pharmacist-Administration-of-Hazardous-Medications.pdf
7 Kennedy K, Vu K, Coakley N, Daley-Morris J, Forbes L, Hartzell R, et al.; Nursing Guideline Development Group. Safe handling of hazardous drugs. Cancer Care Ontario; mars 2022 [consulté le 4 janvier 2024]. Disponible à: https://www.cancercareontario.ca/en/guidelines-advice/types-of-cancer/2161
8 Bédard S, Bertrand G, Bussières JF, Chevrette A, Chouinard A, Ferland G, et al. Guide de prévention – manipulation de médicaments dangereux. Association paritaire pour la santé et la sécurité au travail du secteur affaires sociales; 2021 [consulté le 4 janvier 2024]. Disponible à: http://asstsas.qc.ca/publication/guide-de-prevention-manipulation-securitaire-des-medicaments-dangereux-gp65
9 Gurusamy KS, Best LM, Tanguay C, Lennan E, Korva M, Bussières JF. Closed-system drug-transfer devices plus safe handling of hazardous drugs versus safe handling alone for reducing exposure to infusional hazardous drugs in healthcare staff. Cochrane Database Syst Rev. 2018; 3(3):CD012860.
PubMed PMC
10 Pinet E, Cirtiu CM, Caron N, Bussières JF, Tanguay C. Canadian monitoring program of the surface contamination with 11 antineoplastic drugs in 124 centers. J Oncol Pharm Pract. 2023;30(1):19–29.
Crossref PubMed
11 Palamini M, Floutier M, Gagné S, Caron N, Bussières JF. Evaluation of decontamination efficacy of four antineoplastics (ifosfamide, 5-fluorouracil, irinotecan, and methotrexate) after deliberate contamination. J Occup Environ Hyg. 2021;18(2):43–50.
Crossref
12 Queruau Lamerie T, Nussbaumer S, Décaudin B, Fleury-Souverain S, Goossens JF, Bonnabry P, et al. Evaluation of decontamination efficacy of cleaning solutions on stainless steel and glass surfaces contaminated by 10 antineoplastic agents. Ann Occup Hyg. 2013;57(4):456–69.
13 Soubieux A, Palamini M, Tanguay C, Bussières JF. Evaluation of decontamination strategies for cyclophosphamide. J Oncol Pharm Pract. 2020;26(2):413–22.
Crossref
14 Simon N, Guichard N, Odou P, Decaudin B, Bonnabry P, Fleury-Souverain S. Efficiency of four solutions in removing 23 conventional antineoplastic drugs from contaminated surfaces. PLoS One. 2020; 15(6):e0235131.
Crossref PubMed PMC
Adresse de correspondance: Jean-François Bussières, CHU Sainte-Justine, 3175, chemin côte Sainte-Catherine, Montréal QC H3T 1C5, Courriel: jean-francois.bussieres.hsj@ssss.gouv.qc.ca
Conflits d’intérêts: Aucun déclaré.
Financement: Aucun reçu.
Soumis: 15 janvier 2024
Accepté: 5 mai 2024
Publié: 9 octobre 2024
© 2024 Canadian Society of Hospital Pharmacists | Société canadienne des pharmaciens d’hôpitaux
Canadian Journal of Hospital Pharmacy, VOLUME 77, NUMBER 4, 2024