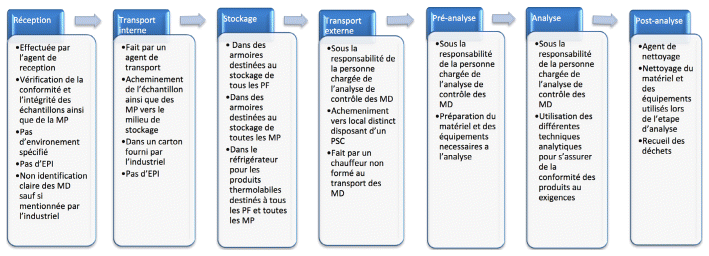
FIGURE 1 Cartographie du processus. EPI : équipements de protection individuelle; MD : médicaments dangereux; MP : matière première; PF : produits finis; PSC : poste de sécurité cytotoxique.
Feriel El Kara, Yassine Mokni, Sarra Ouertani, Emna Amira, Sonia Sebai et Kaouther ZribiComment citer cet article : El Kara F, Mokni Y, Ouertani S, Amira E, Sebai S, Zribi K. Analyse des risques, par la méthode AMDEC, du circuit de contrôle des médicaments dangereux. Can J Hosp Pharm. 2025;78(2):e3631. doi: 10.4212/cjhp.3631
RÉSUMÉ
Contexte
La gestion des risques s’inscrit dans le programme d’amélioration de la qualité et de la sécurité de la prise en charge médicamenteuse.
Objectifs
Cartographier le processus de contrôle des médicaments dangereux (MD), évaluer les risques du circuit de contrôle et définir les actions correctives à mettre en place pour sécuriser le circuit au sein d’un laboratoire de contrôle des médicaments.
Méthodologie
Une étude analytique a été réalisée, sur une période de 6 mois, dans le Laboratoire National du Contrôle des Médicaments en Tunisie. L’analyse des risques a été réalisée par la méthode AMDEC (analyse des modes de défaillance, de leurs effets et de leur criticité).
Résultats
Au total, 53 modes de défaillance et 3 niveaux de criticité ont été détectés en utilisant le diagramme d’Ishikawa et la méthode des 5M (matière, milieu, méthode, matériel, main d’œuvre).Trente-trois étaient de criticité majeure, 14 de criticité modérée et 6 de criticité mineure. Le contrôle des MD est donc un processus de criticité importante (Cmoy : 31,9), ce qui a imposé la mise en place d’un plan d’action efficace afin de réduire le niveau de criticité à faible (Cmoy : 10,4).
Conclusion
Le processus de contrôle des MD était complexe et était associé à un niveau de risque élevé. Après analyse des causes possibles et des obstacles préexistants, un plan d’action a été élaboré. Le suivi des actions reste primordial à la maîtrise de ce processus. Un département spécialisé est à envisager en cas d’augmentation de l’activité, notamment avec l’arrivée des thérapies innovantes qui nécessitent plus de restrictions au cours de la manipulation.
Mots-clés: analyse des risques, sécurisation, contrôle, médicaments dangereux, analyse des modes de défaillance, de leurs effets et de leur criticité, AMDEC
ABSTRACT
Background
Risk management is one aspect of improving the quality and safety of medication care.
Objectives
To map the process of monitoring hazardous drugs, assess the risks of the monitoring cycle and identify corrective actions to be implemented to ensure the safety of the cycle within a drug monitoring laboratory.
Methods
An analytical study was conducted over a period of 6 months in Tunisia’s national drug monitoring laboratory. The risk analysis was carried out using the failure modes and effects analysis (FMEA) method.
Results
A total of 53 failure modes and 3 critical levels were detected using the Ishikawa diagram and the 5M method (equipment environment, methods, materials, workforce). Thirty-three of the failure modes were of major criticality, 14 of moderate criticality and 6 of minor criticality. Overall, hazardous drug monitoring was found to be a high criticality (Cavg: 31.9) process, which required the implementation of an effective action plan in order to reduce the level of criticality to minor (Cavg: 10.4).
Conclusion
The hazardous drug monitoring process was complex and was associated with a high level of risk. After analyzing possible causes and pre-existing obstacles, an action plan was developed. Monitoring the elements of the action plan remains essential to controlling this process. A specialized department may be considered in the event of an increase in activity, for example with the surge of innovative therapies that require more restrictions during handling.
Keywords: risk analysis, safety, monitoring, hazardous drugs, failure modes and effects analysis, FMEA
L’institut national pour la sécurité et la santé au travail (National Institute for Occupational Safety and Health (NIOSH)), dans sa dernière version validée, répartit les médicaments dangereux (MD) en trois groupes : les médicaments antinéoplasiques, les médicaments non antinéoplasiques qui répondent à un ou plusieurs des critères du NIOSH pour un MD et les médicaments qui présentent un risque sur la reproduction. Cette liste NIOSH est mise à jour périodiquement1. L’ébauche de 2020 est en attente d’approbation et se limite à deux groupes : les médicaments à risque sur la reproduction seraient transférés à la partie annexe1. Ces médicaments présentent un risque sur la santé des manipulateurs professionnels2. Il est donc important de prévoir un circuit permettant de sécuriser leur manipulation aux différents stades.
La gestion des risques s’inscrit dans le programme d’amélioration de la qualité et de la sécurité de la prise en charge médicamenteuse prévu par l’arrêté français du 6 avril 20113,4. Il s’agit d’approches complémentaires et souvent très imbriquées5. Le circuit de préparation, de contrôle et de dispensation des MD implique une gestion des risques adaptée, d’autant plus que les conséquences portent non seulement sur la sécurité des soins, mais aussi sur la qualité des médicaments.
Ainsi, dans le cadre de la démarche d’amélioration continue de la qualité des médicaments, notamment celle des médicaments anticancéreux, la sécurisation du circuit de contrôle des médicaments était l’un des objectifs prioritaires au sein du Laboratoire de Contrôle des Médicaments (LCM).
Au cours de ces dernières années, une augmentation du nombre de dossiers traités des MD au LCM a été observée. En effet, les demandes d’Autorisation de mise sur le marché (AMM) ont augmenté suite à l’augmentation de production de génériques de MD, ce qui a augmenté l’activité de contrôle de ces produits. Dans ce contexte, une évaluation spécifique, pluriprofessionnelle des risques, selon la méthode AMDEC (analyse des modes de défaillance, de leurs effets et de leur criticité) a été entreprise. L’objectif de ce travail consiste ainsi à cartographier le processus de contrôle des MD, d’évaluer les risques du circuit de contrôle et de définir les actions correctives à mettre en place pour sécuriser le circuit au sein du LCM.
Il s’agit d’une étude analytique qui a été menée, sur une période de 6 mois, dans un LCM ayant pour mission principale le contrôle de la qualité des médicaments. Le LCM représente un établissement public sous la tutelle du ministère de la santé. Le LCM représente la seule instance réglementaire du pays autorisée à contrôler les médicaments, non seulement avant l’obtention de l’AMM mais aussi en post-commercialisation dans le cadre de la campagne nationale de contrôle. La prise en charge des analyses physico-chimiques des médicaments est réalisée au sein du laboratoire de chimie qui a pour principales missions le contrôle de la qualité des médicaments déposés dans le cadre d’une AMM (analyses physico-chimiques des médicaments, en particulier celle des MD, analyses microbiologiques) et la vérification des monographies de contrôle adoptées par l’industrie pharmaceutique, et ce, conformément aux lignes directrices et références internationales, ainsi que la surveillance du marché des médicaments chimiques et autres produits de santé6. Par ailleurs, les MD sont des produits de santé présentant des risques spécifiques. Ils font l’objet de conditions particulières de manipulation et nécessitent une vigilance accrue.
L’AMDEC est une méthode d’analyse des risques a priori inductive qui a pour but de recenser les défaillances potentielles d’un système. Les défaillances sont analysées pour préciser leur criticité, cerner les principales causes et, à la fin, définir des mesures de réduction des risques adaptées. La méthode a évolué et fait l’objet de nombreuses applications7.
Un groupe de travail pluriprofessionnel a été constitué afin d’associer les points de vue des principaux acteurs intervenant directement sur le processus à étudier. L’équipe de travail a été composée comme suit : deux pharmaciennes assistantes hospitalo-universitaires, une assistante de direction, des préparateurs, des résidents en pharmacie hospitalière et industrielle et une qualiticienne formée en méthodes de gestion des risques. Les participants ont reçu une formation sur la méthodologie AMDEC et ont suivi les étapes suivantes :
|
| ||
|
FIGURE 1 Cartographie du processus. EPI : équipements de protection individuelle; MD : médicaments dangereux; MP : matière première; PF : produits finis; PSC : poste de sécurité cytotoxique. | ||
|
| ||
|
FIGURE 2 Analyse des causes des défaillances : diagramme d’Ishikawa. EPI : équipements de protection individuelle; EPC : équipements de protection collective; HPLC : high-performance liquid chromatography; MD : médicaments dangereux; MP : matière première; PF : produit finis; PSC : post de sécurité cytotoxique; UV : ultraviolet | ||
TABLEAU 1 Cotation de la gravité, de la fréquence, de la détectabilité et de la criticité
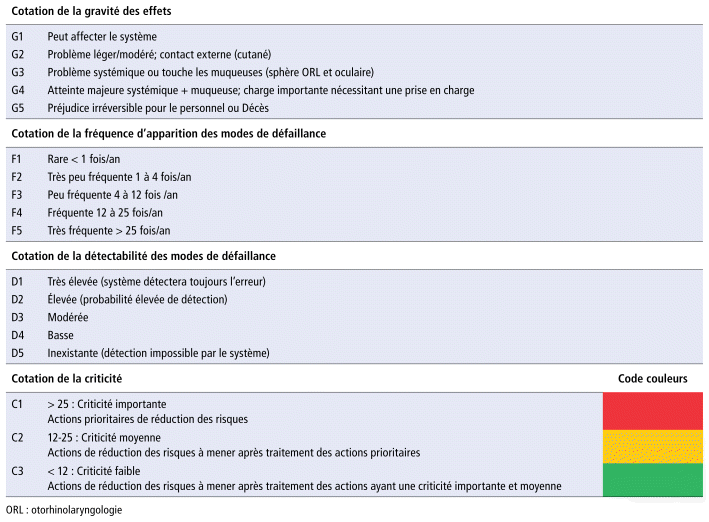
TABLEAU 2 Synthèse des modes de défaillance et de leur criticité
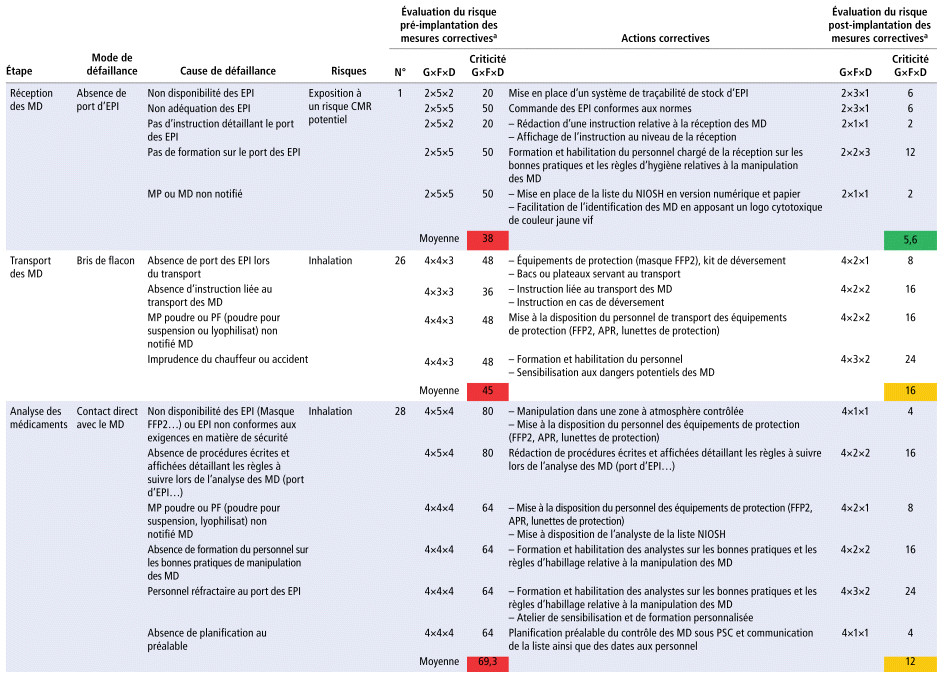
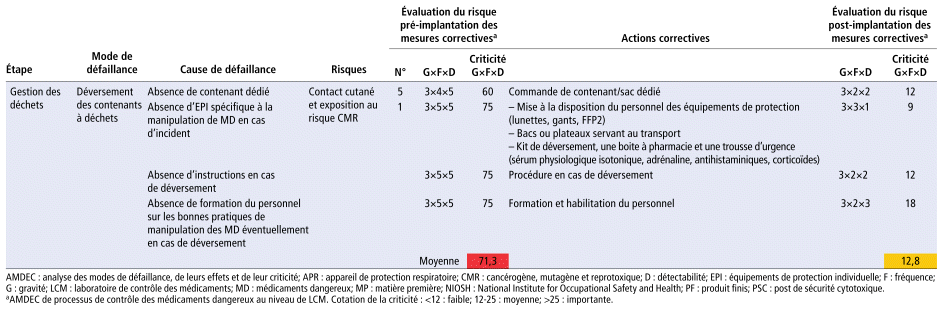
L’ensemble de ces étapes est représenté au niveau du tableau 2.
Les données de cette étude ont été saisies dans un document Microsoft Word, une feuille de calcul Microsoft Excel (Microsoft Corporation) et le logiciel Google Drive (Google LLC).
Le groupe a organisé 15 réunions d’une durée moyenne de 2 heures à chaque fois. Chaque réunion était axée sur un objectif bien déterminé. En parallèle, des entretiens ont permis d’ajuster la méthode entre la qualiticienne, les résidents en pharmacie en charge de la synthèse du travail et le pharmacien référent du service.
Les étapes du processus d’intérêt sont décrites par la figure 1 sous forme de diagramme de flux. Le processus de contrôle des MD a été divisé en 4 étapes, à savoir : réception, transport, analyse des produits finis (PF) ainsi que la gestion de leurs déchets. L’étape de transport a été divisée en transport interne et externe dans le diagramme, le stockage fait partie de l’étape de réception et le processus pré-analyse fait partie intégrante de l’étape analyse des PF.
Par la méthode AMDEC, notre étude a mis en évidence l’existence de 53 risques recensés dans les différentes étapes du circuit des MD. Leur répartition était comme suit : réception (30,2 %), transport (18,9 %), analyse des PF (41,5 %) et gestion des déchets (9,5 %). La répartition des risques associés à chacune des étapes du circuit de contrôle des MD est présentée dans le tableau 2. Parmi les risques recensés, 33 ont été évalués de criticité importante, 14 risques de criticité moyenne et 6 de criticité faible. Les risques de criticité importante concernaient essentiellement l’étape de l’analyse (16) suivie des étapes de réception (10), de transport (5) et de gestion des déchets (2). Les risques de criticité moyenne concernaient les étapes de réception (4) et d’analyse (4) suivies des étapes de transport (3) et de gestion des déchets (3).
Sur l’ensemble du processus, 53 risques ont été recensés. Le tableau 2 précise la valeur des différents paramètres de criticité calculée suivant la formule : C = G × F × D. Elle apparaît selon un code couleur permettant de l’apprécier visuellement. Les criticités moyennes obtenues sont comprises entre 38 et 71. Les modes de défaillance ayant les criticités les plus élevées sont de couleur rouge (tableau 2). Le risque le plus critique concernait le contact cutané et l’exposition au risque cancérogène, mutagène et reprotoxique (CMR) potentiel lors du déversement des contenants à déchets dangereux (moyenne C51 = 71,3). La détermination de la criticité de chaque étape a permis le calcul de leur criticité moyenne. L’exploitation de ces données a permis le calcul de la criticité moyenne globale. Le contrôle des MD était un processus de criticité importante (Cmoy : 31,9).
Les causes de défaillances sont détaillées dans le tableau 2 étape par étape. Elles concernaient essentiellement : l’absence d’identification des MD, l’absence de formation du personnel sur les bonnes pratiques de manipulation des MD et l’absence de procédures écrites et affichées détaillant la technique à suivre à chaque étape du circuit des MD. Elles sont représentées sous forme d’un diagramme « cause-effet » dit d’Ishikawa (figure 2).
À partir des modes de défaillance les plus critiques, plusieurs mesures de réduction des risques ont été proposées par le groupe de travail ainsi que la mise en place effective d’actions correctives prioritaires (tableau 2).
La mise en place effective des actions correctives a été suivie d’une réévaluation des paramètres de fréquence et de détectabilité. Une baisse de la criticité a été notée pour 52 risques parmi 53, soit 98 %. Treize risques importants ont été baissés à une criticité faible (<12) et 20 risques importants ont été baissés à une criticité moyenne (12–25). Après la mise en place d’un plan d’action, une réduction du niveau de criticité à faible (Cmoy : 10,4) a été observée.
Un médicament est considéré comme dangereux si des études faites sur les humains ou les animaux révèlent qu’il comporte une ou plusieurs des 6 caractéristiques suivantes : il est cancérogène, tératogène, génotoxique, toxique pour la reproduction, toxique à faible dose pour un organe ou est un nouveau médicament similaire aux médicaments déclarés dangereux selon les critères précédents 1. Les MD comportent des risques potentiels comme des risques pour le patient, le risque de contamination croisée ou de biocontamination, les risques liés à toute préparation de médicaments cytotoxiques et les risques spécifiques à la manipulation de ces médicaments pour le personnel 9. Des études publiées ont montré que l’exposition à des MD sur le lieu de travail peut avoir des effets aigus et chroniques sur la santé, tels que des éruptions cutanées, des problèmes de reproduction (notamment l’infertilité, des avortements spontanés et des malformations congénitales), et éventuellement des maladies néoplasiques. Le risque pour la santé d’un travailleur dépend du degré d’exposition du travailleur à ces médicaments et de leur toxicité10,11.
L’AMDEC était la méthode utilisée dans notre étude. Il s’agit d’une méthode d’analyse à la fois qualitative et quantitative. Sa démarche visait à identifier les vulnérabilités du processus de contrôle des MD et à élaborer un programme de mesures de réduction des risques adapté, réaliste et priorisé. Par ailleurs, plusieurs études étaient similaires à la nôtre quant à la cartographie du processus, à l’analyse des risques par la méthode AMDEC ou au calcul de criticité12–15. Dans la littérature, peu d’études traitaient le contrôle des MD; certaines études utilisaient l’AMDEC pour l’amélioration de la sécurité du processus de chimiothérapie anticancéreuse14.
L’étude de l’ensemble du processus de contrôle des MD a permis d’avoir une vision globale du fonctionnement du circuit et de décortiquer les différentes étapes les plus à risque. La cartographie du processus a été présentée sous forme d’un diagramme de flux (figure 1). Elle comporte les différentes étapes élémentaires du circuit.
Au total, 53 modes de défaillance et 3 niveaux de criticité ont été détectés en utilisant le diagramme d’Ishikawa et la méthode des 5M (matière, milieu, méthode, matériel, main d’œuvre), plus le management (figure 2). A chaque mode de défaillance, une ou plusieurs causes ont été associées. Certaines causes se sont révélées communes à plusieurs modes de défaillance. Le diagramme d’Ishikawa et les cartographies ont souvent été utilisés dans la littérature lors de la réalisation d’AMDEC, car ils permettent d’obtenir une représentation visuelle claire du processus à analyser13.
Notre étude a montré que dans notre établissement, parmi les risques identifiés, 33 étaient de criticité importante, 14 de criticité moyenne et 6 de criticité faible. Le contrôle des MD est un processus de criticité importante (Cmoy : 31,9), ce qui a imposé la mise en place d’un plan d’action efficace afin de réduire le niveau de criticité à faible (Cmoy : 10,4).
Les risques de criticité importante concernaient essentiellement l’étape de l’analyse des MD (16) suivie de l’étape de réception (10) et de transport (5). Les modes de défaillance inacceptables de niveau 3 (criticité >25) ont fait l’objet de correction immédiate. Les risques de criticité moyenne concernaient les étapes de réception (4) et d’analyse (4) suivies des étapes de transport (3) et de gestion des déchets dangereux (3). Notre étude a utilisé la même méthodologie que celle adoptée par Hurtrel et al.12 En effet, les auteurs ont divisé leur circuit en plusieurs étapes puis calculé la criticité de chaque mode de défaillance pour enfin calculer les moyennes de criticité de chaque étape et la moyenne générale du processus. Néanmoins, ils n’ont pas détaillé les causes de chaque mode de défaillance, à l’inverse de l’étude de Hayat Bonan11.
La détermination des points critiques a permis de définir les priorités d’action. Le tableau 2 rapporte les différentes actions correctives proposées. Ces mesures étaient réparties en plusieurs actions qui ont été priorisées en fonction de la criticité des modes de défaillance mais aussi de leur faisabilité et des besoins en ressources associées. Parmi elles, on peut dénombrer la mise à disposition d’équipements de protection individuelle (EPI) et d’équipements de protection collective (EPC) spécialisés. La formation du personnel a permis l’engagement de groupe et la prise de conscience collective et était définie dans le plan d’amélioration continue. La rédaction de procédures et d’instructions a clarifié certaines étapes, a favorisé l’acceptabilité et a diminué les peurs qui pouvaient exister quant à la manipulation de ces produits. La mise à disposition de la liste NIOSH sous format papier et numérique a facilité l’identification des MD au niveau de la réception et l’information des analystes. Certaines mesures étaient simples à mettre en place (entreposage dans des armoires séparées des autres PF ou d’autres substances de références, mise à disposition de bacs de transports, impression de logo de signalisation du danger CMR), faciles et n’ont pas nécessité l’augmentation du budget. Néanmoins, certaines autres actions étaient difficiles à mener et ont nécessité un temps de commande assez long : achats de gants de protection contre les MD, masques FFP (filtering facepiece), littéralement « pièce faciale filtrante », avec une capacité de filtration de 94 % et 99 % pour le FFP2 et le FFP3, respectivement, surblouses, kit casse (une trousse qui permet de réagir rapidement au déversement afin de prévenir la contamination et les dommages éventuels), sacs poubelles et conteneurs destinés aux déchets des MD.
Sadeghipour et al.15 ont défini les niveaux d’action suivants : pas d’action quand le risque est acceptable et des mesures d’amélioration quand le risque est inacceptable. Ce plan d’action a été suivi par le calcul du risque résiduel.
Le risque d’exposition aux MD est défini en fonction du taux d’exposition à celui-ci. Il peut être quantifié par l’indice de contact cytotoxique (ICC) : ICC = (nR + nA)/nH, où nR représente le nombre de préparations réalisées par une même personne pendant une période déterminée, nA, le nombre d’administrations réalisées par une même personne pendant la même période, et nH, le nombre d’heures de travail de la personne durant la période déterminée.
Si l’ICC est <1, il s’agirait d’une manipulation occasionnelle nécessitant des mesures de prévention individuelles; si 1<ICC<3 (niveau 2), la manipulation est modérée et nécessiterait la mise en place d’une prévention collective (poste de sécurité cytostatique); et si l’ICC>3, il s’agit d’une manipulation intensive qui impose la mise en place d’une unité centralisée9. Dans notre unité, l’ICC était de niveau 2, ce qui a incité la réflexion sur la nécessité de création d’un département distinct destiné à la manipulation des MD. Néanmoins, ce département serait délocalisé de notre local central pour manque d’espace, ce qui engendrerait d’autres risques qui n’ont pas fait partie de notre analyse tels que la réticence du personnel à la délocalisation professionnelle; le transport de certains équipements qui nécessiterait une replanification de leur qualification (appareil de chromatographie en phase liquide à haute performance [HPLC]); la commande du matériel nécessaire au contrôle. Cependant, l’étape de transport était une étape à risque ce qui serait un obstacle éventuel à la décentralisation de cette activité critique. En effet, une analyse globale des risques réalisée par Rousseau et al.16 sur l’activité de sous-traitance de préparations stériles de chimiothérapie a identifié la logistique avec le transport comme étant une étape à risque.
Une AMDEC réalisée dans une industrie pharmaceutique a conclu que la contamination des conditionnements primaire ou secondaire était un risque mineur 17, ce qui n’était pas en concordance avec notre étude. En effet, la contamination résiduelle des conditionnements de PF ou de matière première au niveau de l’étape de réception était un risque moyen et a été pris en compte dans le plan de gestion des risques.
Il a été démontré, également, que l’utilisation d’un dispositif de transfert de médicaments en système fermé réduisait la contamination des surfaces et éventuellement l’exposition des travailleurs aux produits dangereux, mais peut ne pas éliminer complètement l’exposition potentielle18. Ceci pourrait motiver le personnel à travailler sous poste de sécurité cytotoxique afin de réduire le risque d’exposition.
Les limites de cette étude seraient que les modes de défaillance sont spécifiques au processus d’analyse des médicaments du LCM, ce qui peut limiter la généralisation des résultats à d’autres organisations. Cette limite est observée en laboratoire d’analyse des médicaments ainsi qu’en consultation ambulatoire d’oncologie comme décrit par Weingart et al. dans leur étude.19 Un autre point souvent abordé est la subjectivité dans l’évaluation des modes de défaillance et de leur criticité. Les jugements des experts peuvent varier, ce qui peut influer sur la fiabilité des résultats19.
Cette étude a permis de cartographier le processus de contrôle des MD au sein du LCM, mettant l’accent sur les différentes étapes à risques et les acteurs impliqués. L’évaluation des risques a relevé différents points de vulnérabilité. Afin d’y remédier, un plan d’action a été élaboré par l’analyse des causes possibles et des obstacles préexistants. Parmi les actions prévues, la plupart sont déjà réalisées. Le suivi des actions reste primordial à la maîtrise de ce processus. Un département spécialisé reste à envisager en cas d’augmentation de l’activité, notamment avec l’arrivée des thérapies innovantes qui nécessitent plus de restrictions au cours de la manipulation.
1 Hazardous drugs: draft NIOSH list of hazardous drugs in healthcare settings, 2020; procedures; and risk management information. National Institute for Occupational Safety and Health; 2020 [consulté le 20 avril 2024]. Disponible à : https://www.cdc.gov/niosh/docket/review/docket233c/default.html
2 Gestion des médicaments. Médicaments dangereux ou matières dangereuses. Ordre des Pharmaciens du Québec; 2016 [consulté le 20 avril 2024]. Disponible à : https://guide.standards.opq.org/guides/medicaments-dangereux-ou-matieres-dangereuses
3 Arrêté du 6 avril 2011 relatif au management de la qualité de la prise en charge médicamenteuse et aux médicaments dans les établissements de santé. JORF, n° 90, texte n° 14. République Française; 16 avril 2011 [consulté le 20 avril 2024]. Disponible à : https://www.legifrance.gouv.fr/loda/id/JORFTEXT000023865866/2022-04-12
4 ICH Q9 quality risk management [lignes directrices scientifiques]. European Medicines Agency; 2015 [consulté le 20 avril 2024]. Disponible à : https://www.ema.europa.eu/en/ich-q9-quality-risk-management-scientific-guideline
5 Roussel P, Moll MC, Guez P. Méthodes et outils essentiels de la gestion des risques en santé. Étape 1 : Structurer une démarche collective de gestion des risques. Risqu Qual. 2007;4(3):171–9.
6 Service des analyses chimiques. République Tunisienne, Laboratoire National de Contrôle des Médicaments; 2024 [consulté le 20 avril 2024]. Disponible à : http://www.lncm.tn/nos-services/service-chimie
7 Ghrieb Z, Walter-Petrich A, Huang J, Chevret S, Montlahuc C, Resche-Rigon M, et al. Chronologie de la certification ISO 9001:2015 et enquête de satisfaction au sein du centre d’investigations cliniques plurithématique (CIC-P) de l’historique hôpital Saint-Louis en période de pandémie du COVID-19. Therapies. 2024;79(5):519–31.
8 Zellmer WA, Talley R. The literature of pharmacy. Dans : Brown TR, dir. Handbook of institutional pharmacy practice. 4e éd. American Society of Health-System Pharmacy; 2006. https://doi.org/10.1016/j.therap.2023.12.004
9 Recommandations pour la manipulation des médicaments cytotoxiques dans les établissements de santé. Comité de Coordination de Lutte contre les Infections Nosocomiales (CCLIN) SudOuest; 2002.
10 Sahli J, Ghardallou ME, Bougmiza I, Henchiri B, Limam M, Mejdoub R, et al. Évaluation de la sécurité du circuit des médicaments anticancéreux dans un hôpital régional en Tunisie. Pan Afr Med J. 2016;23:30.
11 Hayat Bonan B. Sécurisation du circuit des chimiothérapies en établissement hospitalier : application à la production des médicaments anticancéreux [thèse]. École Centrale des Arts et Manufactures; 2007.
12 Hurtrel F, Beretz L, Renard V, Hutt A. Analyse des risques liés au circuit de gestion et de dispensation des produits en expérimentation clinique par « AMDEC ». Risqu Qual. 2012;10(1):22–30.
13 Boulé M, Lachapelle S, Collin-Lévesque L, Demers É, Nguyen C, Lebel D, et al. Approche commentée par étape pour réaliser une AMDEC dans le cadre du circuit du médicament. Pharm Hosp Clin. 2018;53(4):315–24. https://doi.org/10.1016/j.phclin.2018.05.007
14 Regnier-Gavier O, Beretz L, Gourguillon M, Dumeny E, Fleury B, Reiningerd V, et al. Analyse des modes de défaillances et de leurs effets sur la prise en charge des patients par analgésie contrôlée. Pharm Hosp Clin. 2018;53(4):332–41. https://doi.org/10.1016/j.phclin.2018.08.002
15 Sadeghipour F, Bonnabry P. Méthodologie AMDEC: application à la préparation des anticancéreux. 8e congrès GERPAC; 19 octobre 2005 [consulté le 21 avril 2024]. Disponible à : https://pharmacie.hug.ch/ens/conferences/fspb_method_amdec_gerpac05.pdf
16 Rousseau J, Zribi K, Cotteret C, Marcais A, Winter S, Salguero-Hernandez G, et al. Subcontracting sterile pediatric and adult chemotherapy preparations activity: a global risk analysis. Health Sci Rep. 2022;5(4):e571. https://doi.org/10.1002/hsr2.571
PubMed PMC
17 Tréhel C. Gestion du risque de contamination croisée en industrie pharmaceutique [thèse]. Université Bordeaux 2, UFR des Sciences Pharmaceutiques; 2015.
18 Managing hazardous drug exposures: information for healthcare settings. DHHS (NIOSH) Publication no. 2023–130. Department of Human Health Services, Centers for Disease Control and Prevention, National Institute for Occupational Safety and Health; 2023. https://doi.org/10.26616/NIOSHPUB2023130
19 Weingart SN, Spencer J, Buia S, Duncombe D, Singh P, Gadkari M, et al. Medication safety of five oral chemotherapies: a proactive risk assessment. J Oncol Pract. 2011;7(1):2–6. doi:10.1200/JOP.2010.000064.
PubMed PMC
Adresse de correspondance : Dre Feriel El Kara, Département de physico-chimie, Laboratoire National de Contrôle des Médicaments, 11, Bis, Rue Jbel lakhdhar Bab Saadoun, Tunis, Tunisie, Courriel : elkaraferiel@yahoo.com
Conflits d’intérêts : Aucune déclaration.
Financement : Aucun reçu.
Soumis : 30 avril 2024
Accepté : 6 octobre 2024
Publié : 9 avril 2024
© 2025 Canadian Society of Healthcare-Systems Pharmacy | Société canadienne de pharmacie dans les réseaux de la santé
Canadian Journal of Hospital Pharmacy, VOLUME 78, NUMBER 2, 2025